
电话:029-87679000(总机)
地址:陕西省西安市西五路157号
邮编:710114
网址:www.2yuan.xjtu.edu.cn

电话:029-87679000(总机)
地址:陕西省西安市西五路157号
邮编:710114
网址:www.2yuan.xjtu.edu.cn

放疗(RT)不仅通过诱导DNA双链断裂直接杀伤肿瘤细胞,还能激活免疫反应,将免疫“冷”肿瘤微环境(TME)重塑为炎性或“热”状态。然而,放疗诱导产生的TGF-β和VEGF具有强大的免疫抑制作用,常抵消其免疫激活效应,阻碍抗肿瘤免疫反应,并削弱放疗诱发的远隔效应。针对这一问题,西安交通大学第二附属医院乳腺疾病诊疗中心康华峰教授团队创新性提出放疗联合双抗治疗新策略:逆转免疫抑制,增强抗肿瘤远隔效应。该策略成功解决了因放疗上调VEGF及TGF-β而对肿瘤微环境产生的影响,并显著增强了远隔效应,还为将放疗应用潜力拓展至局部进展期及转移性肿瘤的治疗提供了重要证据。
研究发现,基于靶向VEGF/TGF-β的双特异性抗体Y332D(武汉友芝友生物科技公司研发),结合局部放疗,利用二者的互补机制,成功使免疫原性差、细胞外基质(ECM)丰富且血管生成活跃的肿瘤恢复治疗敏感性。研究表明,在多种小鼠肿瘤模型中,放疗联合Y332D治疗展现出强大的抗肿瘤效果,并能有效消退已建立的自发性肺转移灶。Y332D的关键作用在于阻断TGF-β和VEGF信号通路,从而逆转放疗诱导的多重负面效应,包括TGF-β信号通路过度激活、过度的ECM沉积、上皮-间质转化(EMT)过程、新生血管形成、放射抵抗性及免疫抑制状态。此外,Y332D还进一步增强了放疗对肿瘤微环境的积极影响,将免疫“冷”肿瘤有效转化为免疫“热”肿瘤,形成强大的“原位肿瘤疫苗”。这显著放大了抗肿瘤免疫反应,不仅有效根除了局部肿瘤,更增强了对已建立的自发性肺转移灶的远隔杀伤效应。该研究所开发的联合策略,成功克服了因放疗上调VEGF及TGF-β而对肿瘤微环境产生的负面影响,并显著增强了远隔效应,从而将放疗的应用潜力拓展至局部进展期及转移性肿瘤的治疗。
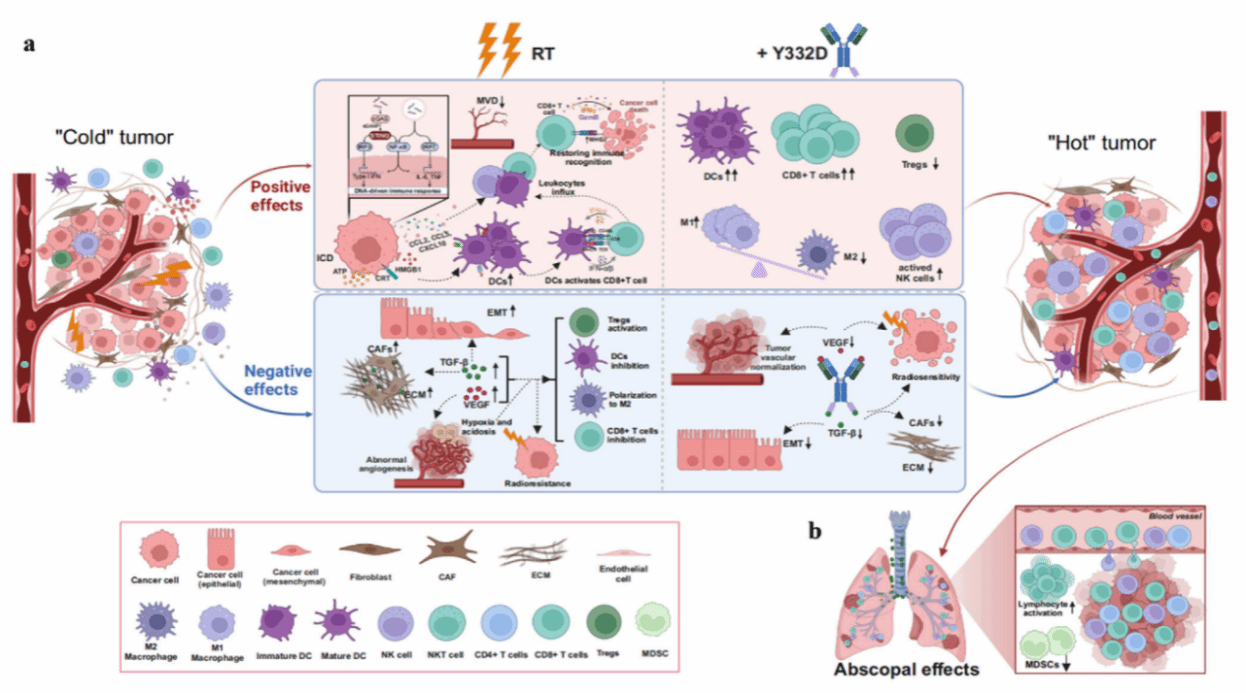
近日,该研究成果以《靶向VEGF/TGF-β双特异性抗体联合局部放疗:促使肿瘤由“冷”转“热”并增强远端效应》(Bispecific Antibody Targeting VEGF/TGF-β Synergizes with Local Radiotherapy: Turning Tumors from Cold to Inflamed and Amplifying Abscopal Effects)为题,发表于国际权威期刊《尖端科学》(Advanced Science,影响因子:14.1)。该论文第一作者为西安交通大学第二附属医院吕丽娟博士,华中科技大学同济医学院附属同济医院肿瘤中心吴孔明教授、西安交通大学第二附属医院康华峰教授和浙江大学第一附属医院代志军教授为共同通讯作者。西安交通大学第二附属医院为通讯单位。
康华峰教授团队长期致力于乳房与胸壁整形修复重建的临床与基础研究,医工交叉融合,纳米药物与功能性探针研发,医学大数据分析等研究领域。团队研究成果在攻克乳腺癌耐药性及推动精准诊疗临床转化方面做出了重要贡献。
论文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202501819